Siempre he tenido una auténtica obsesión por mantenerme al día en las últimas tecnologías y avances científicos que puedan mejorar la vida de mis pacientes. Por eso, cuando escuché hablar del TRG-035, un anticuerpo que promete regenerar dientes perdidos y que muchos ya presentan como el posible fin de los implantes dentales, sentí la necesidad de analizarlo a fondo.

En este artículo comparto, desde una mirada crítica y curiosa, qué hay realmente detrás de esta revolución científica: cómo actúa este fármaco para reactivar los gérmenes dentales dormidos, qué resultados se han obtenido hasta ahora y si de verdad estamos ante el comienzo de una nueva era en odontología.
Avances científicos sobre el TRG-035
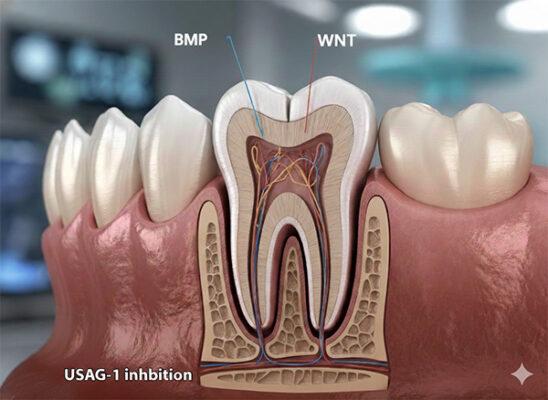
Os comento el Mecanismo de acción: TRG-035 es un anticuerpo monoclonal diseñado para regenerar dientes bloqueando la proteína USAG-1 (siglas en inglés de Uterine Sensitization Associated Gene-1). USAG-1 fue identificada como un inhibidor natural del desarrollo dental, responsable de mantener inactivos los brotes o gérmenes de una potencial “tercera dentición” que permanecen latentes bajo las encías . Al unirse a USAG-1 y neutralizar su función, TRG-035 elimina esta barrera inhibitoria y reactiva los gérmenes dentales dormidos, activando nuevamente las vías de señalización (BMP y Wnt) necesarias para la formación de dientes

En resumen:
- Bloqueo de USAG-1: El fármaco se dirige a USAG-1, que normalmente frena el crecimiento de nuevas piezas dentales. Al bloquear esta proteína, se “desbloquea” el desarrollo de dientes adicionales más allá de la dentición infantil y adulta .
- Reactivación de brotes dentales: Con USAG-1 inhibida, los tooth buds (gérmenes dentales embrionarios) latentes pueden reactivarse y retomar su desarrollo. Esto desencadena un proceso biológico similar al de la formación de los dientes primarios y permanentes, permitiendo la generación de un diente nuevo donde antes no lo había.
- Administración sistémica: TRG-035 se administra vía inyección intravenosa, a diferencia de tratamientos tópicos o implantes. Este método asegura que el anticuerpo alcance la circulación sistémica y las estructuras bucales, interfiriendo en las rutas biológicas pertinentes de forma eficaz . La administración sistémica resulta clave para afectar a los gérmenes dentales dispersos en la mandíbula o el maxilar.
El mecanismo de acción del TRG-035
Resultados preclínicos:
Antes de pasar a ensayos en humanos, TRG-035 fue probado extensamente en animales con resultados muy prometedores. En modelos de laboratorio se observó que una sola dosis del anticuerpo era suficiente para inducir la formación de un diente completamente nuevo:
- En ratones, la inhibición de USAG-1 desencadenó el crecimiento de una pieza dental adicional (una “dentición extra”) sin efectos adversos significativos . De hecho, en ratones modificados genéticamente para carecer de USAG-1 se vio que un germen dentario que normalmente degenera lograba sobrevivir y erupcionar como diente funcional . Estos estudios demostraron que potenciar la señalización BMP/Wnt (vía la ausencia de USAG-1) aumenta el número de dientes formados.
- En hurones, cuya dentición y tamaño de diente son más similares a la humana, el fármaco también provocó el nacimiento de nuevos dientes completos . Los hurones tratados desarrollaron piezas dentales adicionales, confirmando que el efecto no se limitaba a roedores.
- En animales más grandes (p. ej., perros), los experimentos continuaron reforzando la eficacia y seguridad de TRG-035: se reporta que perros tratados lograron hacer crecer dientes totalmente funcionales, capaces de cumplir su función masticatoria . Estos hallazgos en distintas especies de mamíferos evidenciaron la versatilidad del anticuerpo y sentaron las bases para avanzar hacia estudios clínicos en humanos .
Los análisis histológicos de los dientes regenerados en animales mostraron tejidos normales (dentina, esmalte, pulpa y raíz) comparables a los de un diente natural . En todos los casos, los dientes adicionales eran funcionales, erupcionando en la cavidad oral y participando de la mordida sin anomalías aparentes . Estos resultados preclínicos ofrecieron pruebas de concepto sólidas de que la vía USAG-1 es un blanco terapéutico eficaz para promover la odontogénesis, allanando el camino para las pruebas en humanos .
Al día de hoy no existen resultados publicados en humanos, dado que los ensayos clínicos iniciales están en curso. Sin embargo, los investigadores tenían la expectativa de observar por primera vez regeneración dental en humanos durante estas pruebas. Se ha sugerido que, incluso aunque el objetivo primario de la fase I sea solo evaluar seguridad, podría ocurrir la erupción de algún diente nuevo en los voluntarios adultos de forma incidental, lo cual sería un gran hito médico de confirmarse . El Dr. Katsu Takahashi, líder del proyecto, declaró que estaría “contentísimo” si alguno de los primeros pacientes llegase a regenerar un diente durante el ensayo . No obstante, la transición de resultados animales a humanos viene con cautela: expertos independientes señalan que lo observado en animales no siempre se replica en personas, y queda por demostrar que los nuevos dientes humanos puedan reemplazar de forma funcional y estética a las piezas perdidas.
Aplicaciones clínicas previstas
Indicación principal – agenesia dental congénita:
El desarrollo de TRG-035 está enfocado inicialmente en pacientes con hipodoncia u oligodoncia congénita, es decir, personas que nacen con ausencia de múltiples dientes permanentes. En particular, se busca tratar la oligodoncia severa (seis o más piezas ausentes), una condición rara (prevalencia ~0,1%) que conlleva importantes problemas masticatorios desde la infancia . Estos pacientes suelen depender de prótesis dentales o implantes a edades muy tempranas, con impacto negativo en su calidad de vida. El fármaco TRG-035 podría convertirse en una solución revolucionaria para ellos, permitiendo que desarrollen los dientes permanentes que su genética les impidió formar . Dada la gravedad y rareza de la oligodoncia congénita, el Ministerio de Salud japonés ha designado a TRG-035 como medicamento huérfano para esta indicación (hipodoncia severa) en 2025, facilitando su vía regulatoria .
El plan clínico prevé que, tras confirmar la seguridad en adultos, TRG-035 se pruebe en niños pequeños con agenesia dentaria. En concreto, se proyecta incluir a niños de aproximadamente 2 a 7 años con anodoncia u oligodoncia para evaluar la eficacia en inducir la erupción de los dientes que no les salieron de forma natural . El objetivo último es que estos pacientes pediátricos, hoy dependientes de aparatos protésicos, puedan desarrollar una dentadura definitiva funcional gracias al fármaco, corrigiendo el defecto de nacimiento . De esta manera, TRG-035 sería el primer tratamiento curativo para la agenesia dental congénita, un panorama completamente nuevo en odontología pediátrica.
Pérdida dental adquirida:
Si bien la indicación primaria es genética, la regeneración dental que propone TRG-035 también podría aplicarse en el futuro a la pérdida de dientes en adultos por caries, enfermedad periodontal o trauma. En el ensayo de fase I se incluyó intencionadamente a adultos de 30 a 64 años con al menos un molar faltante , con el fin de evaluar seguridad en población general y sentar bases para indicaciones más amplias. Aunque la regeneración en pacientes con pérdida dental adquirida no es la prioridad inicial, existe la posibilidad de que un adulto sano tratado con el anticuerpo llegue a regenerar la pieza perdida, lo que validaría su uso más allá de los casos congénitos . De ocurrir esto, se abriría la puerta a tratar a millones de personas que han perdido dientes a lo largo de su vida, como alternativa natural a las soluciones protésicas convencionales (implantes, puentes, dentaduras). Los investigadores destacan que un enfoque así tendría ventajas notables: el nuevo diente sería propio del paciente, con tejido vivo, capaz de crecer con raíz e integrarse al hueso maxilar tal como un diente original, aportando sensación y respuesta a fuerzas masticatorias.
Tipos de dientes regenerados y funcionalidad:
TRG-035 busca desencadenar la formación de la pieza dentaria que falta independientemente del tipo (incisivo, canino, premolar o molar), ya que actúa sobre el mecanismo general de los brotes dentales. En modelos animales, el fármaco indujo con éxito tanto la aparición de incisivos supernumerarios en ratones como de molares adicionales en hurones y perros , lo que sugiere que su efecto no se limita a una clase particular de diente. La esperanza es que, en humanos, TRG-035 permita reemplazar cualquier diente permanente perdido mediante la erupción de uno nuevo desde el germen latente correspondiente.
En cuanto a la calidad y funcionalidad de los dientes regenerados,
la evidencia preclínica es alentadora. Los dientes adicionales que crecieron en animales tratados no solo tenían la estructura apropiada (dentina revestida de esmalte, con pulpa interna y raíces bien formadas), sino que también erupcionaron en la arcada dental en posición aprovechable y participaron en la masticación normalmente . Los expertos señalan que, de lograrse algo similar en humanos, el diente regenerado debería mimetizarse con la dentición original en estética y función . No obstante, por tratarse de un proceso biológico puede haber variaciones: podría ocurrir que el nuevo diente no salga perfectamente alineado. En tal caso, los investigadores contemplan manejarlo igual que un diente natural desalineado, es decir, mediante ortodoncia o incluso recolocación quirúrgica si hiciera falta . “La ubicación del nuevo diente puede controlarse hasta cierto punto según el sitio de la inyección; y si crece en un lugar equivocado, siempre podemos moverlo con ortodoncia o trasplantarlo”, explicó el Dr. Takahashi . En definitiva, se espera que un diente regenerado por este método sea indistinguible de uno natural en cuanto a apariencia, funcionalidad y conexiones nerviosas, devolviendo al paciente una solución viva y permanente frente a la pérdida dental.
Cronograma de desarrollo y estado actual
Investigación básica (2007–2020):
El concepto de regenerar dientes mediante inhibición de USAG-1 surgió a partir de hallazgos realizados en Japón a fines de la década de 2000. En 2007, el Dr. Katsu Takahashi y su equipo identificaron en modelos murinos una mutación que provocaba “dientes excesivos”: ciertos ratones presentaban un tercer juego de dientes debido a que no se detenía el desarrollo de los brotes dentales . Analizando este fenómeno, se descubrió que la ausencia de la proteína USAG-1 permitía la formación de dientes adicionales. Esto llevó a la hipótesis de que un fármaco bloqueador de USAG-1 podría inducir la regeneración dentaria también en organismos normales . Durante los años siguientes, el equipo de Takahashi profundizó en la biología molecular de la odontogénesis, identificando USAG-1 (también llamada Sostdc1) como un antagonista de BMP/Wnt crucial en la regulación del número de dientes . Estudios genéticos confirmaron la diana: al cruzar ratones carentes de USAG-1 con ratones modelo de agenesia dental, se restauraba la formación de dientes que originalmente faltaban . Con esta base, se desarrollaron los primeros anticuerpos neutralizantes anti-USAG-1 en el laboratorio, demostrando en 2018–2020 que podían rescatar la formación de dientes en animales con mutaciones dentales congénitas .
En mayo de 2020, sobre la base de estos resultados preclínicos exitosos, se fundó la empresa emergente Toregem Biopharma Co., Ltd. (Kyoto, Japón) para llevar la tecnología “medicina de dentición” hacia la clínica . La compañía –una spin-off de la Universidad de Kioto– fue cofundada por la Dra. Honoka Kiso (CEO) y el Dr. Katsu Takahashi (Director de Tecnología), entre otros, con la misión de desarrollar el primer fármaco capaz de “hacer crecer dientes naturales” en pacientes humanos . Durante 2020-2023, Toregem optimizó un anticuerpo monoclonal humanizado (denominado TRG-035) apto para uso clínico, y recopiló evidencia adicional en modelos animales grandes (p. ej. perros y cerdos) como preparación para los ensayos en personas . Paralelamente, en 2021 se publicaron en la revista Science Advances los resultados fundamentales que demostraban que la inhibición de USAG-1 induce la tercera dentición en mamíferos, consolidando el interés científico internacional en esta estrategia.
Ensayos clínicos en humanos:
La primera prueba clínica en humanos (fase I) de TRG-035 inició en Japón a finales de 2024. El 4 de octubre de 2024, investigadores de la Universidad de Kioto comenzaron a administrar el fármaco a voluntarios en el Hospital Universitario de Kioto, marcando el primer ensayo mundial de un medicamento para regenerar dientes perdidos . Esta fase I reclutó a 30 adultos sanos, de 30 a 64 años de edad, cada uno con al menos un diente faltante (un molar) . El objetivo principal es evaluar la seguridad del anticuerpo en humanos y determinar la dosis óptima, por lo que los participantes recibieron dosis intravenosas controladas de TRG-035 bajo estricta monitorización médica . Según el protocolo, el tratamiento se prolongará por unos 11 meses, período durante el cual se observará cuidadosamente si efectivamente llega a emerger un diente nuevo en la zona edéntula de alguno de los pacientes . Cabe señalar que en esta fase inicial no se incluyeron niños con la patología congénita objetivo, dado que la prioridad es establecer primero un perfil de seguridad en adultos.
Hasta octubre de 2025, el ensayo de fase I se encontraba en curso (con una duración prevista aproximadamente hasta fines de 2025). No se han reportado eventos adversos graves hasta el momento en los participantes, según comunicados preliminares, lo cual es alentador dada la naturaleza sistémica del fármaco. Si la seguridad y tolerabilidad son confirmadas, los investigadores planean avanzar a fase II en 2025–2026, esta vez incluyendo a población pediátrica con hipodoncia/oligodoncia congénita para evaluar la eficacia en la erupción de nuevos dientes .
La fase II probablemente analizará la proporción de niños que logran desarrollar los dientes que les faltaban, así como la funcionalidad de los mismos.
Plazos estimados y aprobación:
Dada la alta necesidad no cubierta en pacientes con anodoncia y el apoyo del estado japonés (vía designación de orphan drug), el desarrollo de TRG-035 se está acelerando dentro de lo posible. Los expertos proyectan que, si las pruebas en humanos resultan exitosas, el medicamento podría estar disponible comercialmente hacia el año 2030 . El propio equipo de Toregem comparte este horizonte: su intención declarada es tener el tratamiento listo para ofrecer a niños con agenesia dental a inicios de la próxima década (2030) . Este cronograma implicaría completar las fases clínica restantes y obtener la aprobación en Japón alrededor de 2028–2029, seguida de los procesos de fabricación y distribución. Es posible que TRG-035 siga una ruta regulatoria prioritaria en Japón debido a su condición huérfana, acortando algunos tiempos administrativos. Sin embargo, existen retos importantes que podrían influir en los plazos: por ejemplo, si surgen dudas de seguridad que requieran estudios adicionales, o si se decide expandir las indicaciones (lo que implicaría ensayos más amplios). Además, para su uso fuera de Japón, habría que realizar ensayos multinacionales conforme a exigencias de la FDA (EE. UU.) o la EMA (Europa), lo cual tomaría tiempo extra.
Obstáculos y consideraciones regulatorias:
Como primer fármaco en su tipo, TRG-035 enfrenta un escrutinio riguroso por parte de las autoridades sanitarias. Algunas consideraciones clave incluyen:
Seguridad sistémica:
Dado que USAG-1 interactúa con vías generales de crecimiento (BMP/ Wnt), es fundamental demostrar que bloquearla no cause efectos colaterales indeseados en otros órganos. Los estudios en animales mostraron que ciertos anticuerpos anti-USAG-1 que afectaban simultáneamente la señalización Wnt provocaron problemas en el desarrollo corporal. Por ello, TRG-035 fue diseñado para interferir mayormente con la ruta BMP, buscando minimizar efectos fuera de la odontogénesis . Aun así, las agencias reguladoras exigirán un amplio seguimiento de posibles impactos en huesos, glándulas u otros tejidos durante los ensayos clínicos.
Eficacia comprobada:
Será necesario aportar evidencia sólida de que el fármaco efectivamente logra la erupción de nuevos dientes funcionales en humanos. Dado que no hay precedente, los criterios de éxito podrían incluir radiografías que muestren la formación del germen dental y la salida del diente, así como evaluaciones de mordida, alineación y dureza del esmalte en los nuevos dientes. Estos resultados deben compararse contra el estándar actual (que, en ausencia de tal fármaco, sería la colocación de implantes o prótesis) para convencer a las autoridades de su beneficio clínico.
Control de la erupción dental:
Un desafío único es controlar dónde y cómo emerge el diente regenerado. Si bien en principio el nuevo diente debería ocupar el alvéolo vacío de la pieza perdida, las autoridades querrán asegurarse de que no aparezcan dientes ectópicos en lugares indeseados. Takahashi ha argumentado que la localización puede dirigirse mediante la inyección cerca del sitio objetivo, pero esto tendrá que confirmarse en los ensayos . También se monitoreará que no se formen dientes supernumerarios en exceso (por ejemplo, que un paciente desarrolle más piezas de las necesarias).
Duración del efecto:
Otro aspecto es si una ronda de tratamiento basta para regenerar el diente o si harían falta múltiples dosis. La fase I está evaluando una pauta de administración de varios meses ; si se constata un rebrote dental, habrá que decidir si el tratamiento se detiene al formarse el diente o si se continúa para asegurar maduración. Este régimen óptimo tendrá que definirse de cara a la aprobación.
Producción y calidad:
Al ser un medicamento biotecnológico (anticuerpo monoclonal), TRG-035 deberá cumplir con estrictos estándares de fabricación (consistencia lote a lote, pureza, estabilidad). Toregem posiblemente deba asociarse con compañías farmacéuticas con capacidad industrial o subcontratar fabricantes GMP para producir suficientes dosis con calidad aprobada una vez se acerque la fase III y la comercialización.
Costo y acceso:
Si se aprueba, un posible obstáculo será el costo elevado típico de las terapias biológicas innovadoras. Como medicamento huérfano, podría tener un precio alto, por lo que habrá debate sobre cómo incorporarlo en los sistemas de salud y seguros. La compañía podría buscar subsidios o colaboraciones gubernamentales para facilitar el acceso, especialmente dado el beneficio en población pediátrica.
A pesar de estas incógnitas, la visión de los desarrolladores es optimista: “lograr la primera medicina regenerativa dental del mundo y que ‘hacer crecer dientes’ sea una opción clínica real en esta década”, declararon representantes de Toregem . Si todo progresa favorablemente, en unos años podríamos estar ante una terapia aprobada que inaugure una nueva era en odontología, desterrando el miedo a la pérdida dental permanente.
Empresas e instituciones involucradas en el desarrollo
El proyecto TRG-035 se origina de una colaboración academia-industria en Japón, con varios actores clave:
Toregem Biopharma Co., Ltd.:
Es la empresa biotecnológica responsable de desarrollar y eventualmente comercializar el anticuerpo TRG-035. Toregem fue fundada en 2020 como startup derivada de la Universidad de Kioto, con sede en la ciudad de Kioto . Su creación fue liderada por la Dra. Honoka Kiso (CEO de Toregem) y el Dr. Katsu Takahashi (cofundador y director científico) entre otros, contando también con el Dr. Katsu Takahashi como científico jefe de tecnología (CTO) . La visión de la compañía es “la realización de una sociedad donde la gente no tema perder sus dientes”, enfocándose en una “medicina de regeneración dental” que permita al paciente volver a crecer sus propios dientes perdidos .

Toregem ha reunido inversión y apoyo institucional en Japón (por ejemplo, ha sido seleccionada en programas de promoción de fármacos innovadores y ha exhibido sus avances en congresos biotecnológicos como BioJapan 2025 ). Como empresa joven de biotecnología, es probable que busque alianzas estratégicas con laboratorios más grandes para las fases finales de desarrollo y distribución global, aunque hasta 2025 no se han anunciado pactos de licencia internacional específicos.
Equipo científico (Universidad de Kioto y colaboradores):
El desarrollo de TRG-035 se basa en décadas de investigación académica liderada por el Dr. Katsu Takahashi, un dentista e investigador japonés. Takahashi se desempeña como Jefe de Cirugía Oral en el Instituto de Investigación Médica del Hospital Kitano (Osaka) y fue profesor asociado en la Facultad de Medicina de la Universidad de Kioto, donde condujo la mayor parte de la investigación preclínica . Su equipo incluye a especialistas en odontología, biología del desarrollo y biotecnología de diversas instituciones: por ejemplo, científicos del Instituto de Investigación de Proteínas de la Universidad de Osaka contribuyeron al diseño y producción del anticuerpo monoclonal , mientras que investigadores de la Universidad de Fukui participaron en los estudios de eficacia en modelos animales . Esta colaboración multidisciplinaria académicoempresarial fue crucial para trasladar el hallazgo básico (el papel de USAG-1) hacia un candidato farmacéutico viable.
Hospital Universitario de Kioto:
Es la institución donde se está llevando a cabo el ensayo clínico de fase I en humanos. El Departamento de Odontología y Cirugía Oral del Hospital de la Universidad de Kioto, en conjunto con la Facultad de Medicina de dicha universidad, está a cargo de las pruebas clínicas . Esto garantiza un entorno de máxima calidad para la investigación clínica, contando con comités éticos, laboratorios de análisis y personal capacitado en ensayos de medicamentos. La participación del Hospital Universitario también indica que la Universidad de Kioto respalda fuertemente el proyecto, dándole visibilidad y recursos hospitalarios.
Gobierno y entes regulatorios:
El Ministerio de Salud, Trabajo y Bienestar de Japón (MHLW) ha mostrado interés en el desarrollo de TRG-035, otorgándole en septiembre de 2025 la designación de fármaco huérfano para “hipodoncia congénita severa” . Esta designación proporciona incentivos (apoyo en protocolización, subsidios, exención de tasas, exclusividad de mercado por 7 años tras aprobación) que facilitan el desarrollo. Asimismo, la Pharmaceuticals and Medical Devices Agency (PMDA) de Japón colabora en orientar los requisitos de los ensayos clínicos y la futura solicitud de aprobación. No se han anunciado aún colaboraciones con agencias fuera de Japón; es previsible que, de superar la fase II/III en Japón, Toregem busque la aprobación en otros mercados grandes, sea mediante ensayos propios o asociándose con farmacéuticas internacionales.
En conjunto, el ecosistema que impulsa a TRG-035 abarca desde la ciencia básica universitaria hasta el emprendimiento biotecnológico y el apoyo gubernamental. La sinergia entre la Universidad de Kioto (origen del conocimiento) y Toregem Biopharma (vehículo de desarrollo) ha sido destacada como un modelo de innovación translacional. El Dr. Takahashi, por ejemplo, simultáneamente ocupa roles clínicos (en hospital) y empresariales (CTO de Toregem), asegurando que la perspectiva médica y la comercial estén alineadas . Este proyecto también ha involucrado a instituciones privadas y públicas en aspectos específicos, como laboratorios de proteínas, centros de desarrollo de modelos animales y clínicas dentales para asesoría. A medida que el fármaco avance, es posible que más actores (por ejemplo, asociaciones de pacientes con anodoncia, colegios odontológicos, etc.) se involucren en difusión y futuros estudios de seguimiento.
Comparación con otras tecnologías de regeneración dental
El enfoque de regeneración dental mediante un fármaco (TRG-035) es pionero a nivel mundial, pero existen otros abordajes en desarrollo para solucionar la pérdida de dientes. A continuación se comparan las características, estado y perspectivas de TRG-035 frente a las principales estrategias alternativas de regeneración dental:
TRG-035 (anticuerpo anti-USAG-1):
Consiste en una terapia molecular que estimula la dentición natural del paciente mediante la reactivación de gérmenes dentales latentes. Se administra de forma no invasiva (inyección) y promueve que el organismo genere un diente nuevo por sí mismo . Actualmente es la única tecnología en ensayos clínicos en humanos para regeneración de piezas dentales perdidas (fase I iniciada en 2024) . Su principal ventaja es que no requiere cirugías ni cultivos celulares complejos: aprovecha los mecanismos de desarrollo intrínsecos del cuerpo, resultando en dientes biológicamente propios (con raíz, ligamento periodontal y sensibilidad) . Además, podría aplicarse de forma relativamente sencilla a múltiples dientes si funciona (vía varias inyecciones). Como desafíos, TRG-035 debe demostrar que puede controlar la formación del diente (posición adecuada, sin efectos fuera de la boca) y que es seguro a largo plazo al interferir en vías de crecimiento. También enfrenta las barreras regulatorias de cualquier nuevo fármaco biológico, debiendo pasar por todas las fases de pruebas y aprobación antes de su adopción clínica rutinaria.
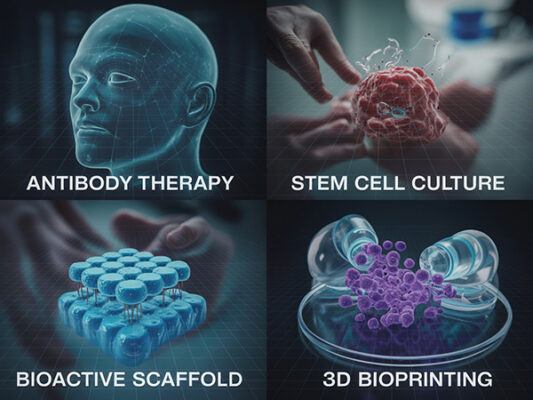
Terapias con células madre y bioingeniería dental:
Engloban los intentos de cultivar nuevos dientes a partir de células vivas del paciente. Un enfoque representativo es la generación de un germen dental en el laboratorio: por ejemplo, en 2025 científicos del King’s College de Londres lograron cultivar un diente humano rudimentario in vitro usando células madre del propio paciente . Este mini-órgano dental creció en condiciones controladas imitando el desarrollo embrionario, gracias a un andamiaje biocompatible que permitió a las células organizarse gradualmente en estructura dental . El resultado fue un diente de laboratorio con tejido vivo y características de un diente real (dentina, pulpa, etc.) . En el futuro, esto abre dos posibilidades: trasplantar directamente células madre estimuladas al alveolo dental para que formen un diente in situ, o implantar el germen dental cultivado en laboratorio en la mandíbula para que termine de madurar allí . La ventaja de la vía celular es que podría generar dientes de repuesto personalizados usando las propias células del paciente, evitando rechazos y logrando reemplazos anatómicamente correctos . Ya se demostró en animales que dientes bioingenierizados pueden integrarse con el hueso y encía, funcionando como dientes naturales . Sin embargo, ninguna terapia celular para cultivar dientes completos ha llegado a ensayos clínicos aún; por ahora son investigaciones de laboratorio y experimentos en animales. Sus retos incluyen la gran complejidad y costo (se requiere extraer células madre del paciente, cultivar el órgano dental en condiciones estériles especiales, y luego cirugía para implantarlo). También debe garantizarse que el diente cultivado se desarrolle con la forma y tamaño correctos y se conecte adecuadamente al nervio y vasos del paciente. A corto plazo, es un enfoque prometedor pero en etapa inicial – los científicos estiman que podrían pasar uno o dos decenios antes de ver dientes cultivados disponibles para pacientes, a medida que la bioingeniería organoide y la medicina regenerativa avancen.
Andamiajes bioactivos y factores de crecimiento:
Esta estrategia busca regenerar estructuras dentales perdidas usando biomateriales implantables que guían a las células del propio paciente. Se utilizan scaffolds (andamios) porosos hechos de materiales biocompatibles, a veces cargados con factores de crecimiento o células, que se colocan en el área del diente dañado o faltante. En el caso de pérdida total del diente, teóricamente un andamio con la forma del diente podría servir de molde donde las células circundantes crezcan formando un nuevo diente. En la práctica, por ahora los andamiajes se han aplicado más en regeneración parcial: por ejemplo, se han usado con cierto éxito para regenerar el tejido pulpar en dientes con endodoncia (reemplazando la pulpa necrosada por tejido vivo nuevo) , o para fomentar la regeneración de hueso alveolar en defectos periodontales. Aún no hay evidencia de que un andamiaje por sí solo pueda regenerar una corona dental completa con esmalte, ya que el esmalte lo producen exclusivamente los ameloblastos durante el desarrollo embrionario. No obstante, se investiga la combinación de scaffolds con células madre dentales para intentar formar organoides de diente. La ventaja de los andamiajes bioactivos es su enfoque local: pueden insertarse en el hueco del diente perdido o dentro de un diente dañado, liberando señales bioquímicas que atraen células madre endógenas y regeneran tejido in situ. Son relativamente seguros y ya se emplean variantes en odontología regenerativa (p. ej. matrices de colágeno con factores para regenerar ligamento periodontal). Su desventaja es que, por ahora, solo logran regenerar componentes individuales (dentina, pulpa, hueso) mas no recrear la compleja organización de un diente completo con esmalte funcional. Para lograr una pieza íntegra, los andamios tendrían que combinarse con técnicas de células madre o estímulos muy precisos que aún se están desarrollando. En resumen, los scaffolds son una herramienta valiosa en odontología regenerativa incremental (reparación de partes de dientes), pero la creación de un diente entero sobre un andamiaje sigue siendo un objetivo no alcanzado.
Bioimpresión 3D de dientes:
La bioimpresión 3D aplica las tecnologías de impresión capa-porcapa con “biotinta” (mezcla de células vivas y biomateriales) para fabricar tejidos u órganos. En odontología, se vislumbra usar bioimpresión para construir la forma de un diente extrayendo células del paciente, mezclándolas en hidrogel, y imprimiéndolas con la geometría del diente necesario. Esta técnica permitiría, en teoría, obtener un “borrador” de diente personalizado que luego maduraría y se mineralizaría para volverse funcional. Actualmente, la bioimpresión ha logrado prototipos de tejido óseo y cartilaginoso, pero un diente completo implica imprimir múltiples tipos de células (ameloblastos, odontoblastos, etc.) en una arquitectura precisa. Algunos investigadores hablan de imprimir andamios celulares que replican la estructura de un diente e inducen su funcionalidad . En la práctica, la bioimpresión dental está en fase de experimentación básica: se han imprimido pequeñas piezas de dentina y se investiga la impresión de tejido pulpar para restauraciones endodónticas , pero no hay ensayos en humanos aún. Una posibilidad futurista es que las clínicas cuenten con mini-laboratorios de bioimpresión para generar tejidos dentales de reemplazo bajo demanda . Esto revolucionaría la práctica odontológica: “la frase ‘necesitas un implante’ podría ser reemplazada por ‘te imprimiremos un diente nuevo’”, como señala un artículo de divulgación . Entre las ventajas del enfoque está la precisión geométrica – se puede diseñar digitalmente la anatomía dental ideal antes de imprimir – y la posibilidad de producir estructuras complejas en poco tiempo. No obstante, los desafíos son inmensos: lograr que las células impresas sobrevivan y se diferencien correctamente, inducir la mineralización del esmalte (uno de los mayores retos), y dotar al constructo de vascularización y inervación para que el diente impreso cobre vida tras implantarlo. Por ahora, la bioimpresión dental es más una visión a largo plazo que una realidad cercana, pero complementa los esfuerzos de regeneración al aportar herramientas de fabricación de alta resolución.
Otros enfoques emergentes:
Además de las categorías anteriores, existen líneas de investigación adicionales buscando la regeneración o reparación dental:
- La terapia génica se explora para casos de mutaciones que causan agenesia dental. Por ejemplo, usando CRISPR/Cas9 podría intentarse corregir genes defectuosos (como WNT10A o PAX9) en células madre del paciente, para restaurar su capacidad de formar dientes. También se ha propuesto editar genes para reducir la respuesta inmunológica y facilitar la integración de dientes regenerados implantados . Estas aplicaciones están en etapas preliminares y se enfrentan al dilema de cómo administrar la terapia génica de forma localizada solo a la región bucal.
- El uso de moléculas pequeñas o péptidos es otra vía: por ejemplo, se ha investigado un péptido derivado de amelogenina (proteína del esmalte) que, aplicado sobre dientes con caries incipientes, ayuda a regenerar y remineralizar el esmalte perdido. Esto no “crea” un diente nuevo, pero sí regenera tejido duro dentro de un diente existente. De igual modo, factores de crecimiento como BMP-7 o FGF-2 se han utilizado en geles para estimular la reparación de defectos óseos o pulpares en la boca. Son terapias complementarias que buscan regenerar componentes dentales y podrían integrarse en protocolos mayores (por ejemplo, usar factores de crecimiento junto con un germen dental implantado para favorecer su desarrollo).
- La fotoestimulación con láser de baja potencia ha mostrado inducir respuestas regenerativas en tejidos dentales. Investigaciones del último decenio descubrieron que ciertos láseres fríos pueden activar células madre de la pulpa dental para formar dentina reparativa. Esto dio lugar a experimentos de regeneración de dentina in vivo mediante la simple irradiación láser de cavidades, aunque está aún en evaluación clínica. Nuevamente, esto atañe a la reparación de un diente dañado, no a la creación de uno nuevo, pero ilustra la diversidad de técnicas en el arsenal regenerativo.
En comparación con todas estas alternativas, TRG-035 destaca por su nivel de avance (ya en fase clínica) y por aprovechar un mecanismo evolutivo latente en los mamíferos (la tercera dentición inhibida).
Mientras que muchas de las otras estrategias requieren manipular células o tejidos fuera del cuerpo, el enfoque con el anticuerpo es in vivo y relativamente sencillo de aplicar. Expertos independientes han señalado que el grupo de Takahashi (TRG-035) está marcando el camino en la regeneración dental, situándose por delante de otros grupos globales con objetivos similares . No obstante, también enfatizan que “la carrera para regenerar los dientes humanos no es un esprint corto, sino una serie de ultramaratones” – es decir, tomará varios enfoques, muchos años y probablemente la combinación de tecnologías para finalmente hacer común la regeneración total de dientes en clínica. En conclusión, TRG-035 representa un hito innovador y complementa a las demás líneas de investigación: es posible que en el futuro cercano veamos una convergencia de terapias (moleculares, celulares y de ingeniería de tejidos) para lograr el objetivo último de que ningún ser humano deba quedarse sin sus dientes naturales.
Mi conclusión:
Después de analizar toda la evidencia disponible, creo que el TRG-035 representa un avance apasionante, pero aún lejano de sustituir a los implantes dentales. Los resultados preclínicos son prometedores y abren una puerta real a la regeneración biológica de dientes, aunque todavía estamos en una fase muy inicial en humanos. La ciencia parece avanzar en la dirección correcta, pero harán falta años de investigación para confirmar su seguridad y eficacia. Por ahora, los implantes siguen siendo la mejor y más predecible solución para reemplazar dientes perdidos.
Y quiero cerrar con un guiño a esta investigación, por que de algún modo, mientras escribía este post pensaba en ello:
parece existir una «relación» con nuestra ciudad, Tarragona.
A menudo cuando hablamos de Tarragona escribimos TRG 😉
¿Llegará a Tarragona el TRG-035? Ya veremos.
Referencias:
- K. Takahashi et al., “Development of a new antibody drug to treat congenital tooth agenesis,” J. Oral Biosci. 66(4):1-9 (2024) .
- Luminance Dentaire – “Japanese Scientists Begin Human Trials for Tooth Regrowth Drug” (Blog, 1 Jun 2025) .
- SWI SwissInfo – “Investigadores japoneses prueban un fármaco para regenerar dientes” (AFP, 14 Dic 2024) .
- The Cherry Health – “Regeneración dental: la tecnología que promete devolverte tus dientes perdidos” (Blog, 2025) .
- El Confidencial – “Descubren un nuevo tratamiento para regenerar los dientes perdidos en adultos” (28 Jul 2025) .
- Gizmodo en Español – “¿Regeneración de dientes humanos? Un desafío evolutivo y tecnológico” (24 Ene 2025).
Toregem Biopharma – “Anti-USAG-1 Antibody TRG035 Designated as Orphan Drug (Japan)” (Nota de prensa, 29 Sep 2025).
Bibliografía consultada:
- Japan Begins Human Trials for Tooth Regrowth Drug TRG-035
https://luminancedentaire.ca/japanese-scientists-human-trials-tooth-regrowth-drug/
- Development of a new antibody drug to treat congenital tooth agenesis – PubMed
https://pubmed.ncbi.nlm.nih.gov/39389160/
- Investigadores japoneses prueban un fármaco para regenerar dientes – SWI swissinfo.ch
https://www.swissinfo.ch/spa/investigadores-japoneses-prueban-un-f%C3%A1rmaco-para-regenerar-dientes/88591492
- Regeneración dental: la tecnología que promete devolverte tus dientes perdidos – The Cherry Health
https://thecherryhealth.es/clinicas-dentales/regeneracion-dental/
- New drug to regenerate lost teeth | KYOTO UNIVERSITY
https://www.kyoto-u.ac.jp/en/research-news/2021-03-31
- Toregem’s Anti-USAG-1 Antibody “TRG035” Designated as an Orphan Drug by Japan’s Ministry of
- Health, Labour and Welfare for the Treatment of Severe Congenital Oligodontia – Toregem BioPharma Co., Ltd.
https://toregem.co.jp/en/archives/8409
- Japanese Scientists Begin Human Trials for Tooth Regrowth Drug | Concierge Dental
https://conciergedentalgroup.com/blog/tooth-regrowth-drug/
- Toregem BioPharma Co., Ltd. – For the realization of a society where people are not afraid of losing their teeth
https://toregem.co.jp/en/
- Descubren un nuevo tratamiento para regenerar los dientes perdidos en adultos
https://www.elconfidencial.com/tecnologia/novaceno/2025-07-28/investigacion-ciencia-descubrimiento-regeneraciondientes_4114609/
- ¿Regeneración de dientes humanos? Un desafío evolutivo y tecnológico
https://es.gizmodo.com/regeneracion-de-dientes-humanos-un-desafio-evolutivo-y-tecnologico-2000145646
Dra. Montse Timoneda Cervantes
Directora médica en Clínica Dental Montse TimonedaDesde muy joven la Dra. Montse Timoneda manifestó una gran pasión por el Oficio de Odontólogo, cuando con solo 14 años lo descubrió en su primera visita al dentista. Actualmente la Dra. Timoneda desarrolla su actividad desde hace más de veinte años en su Clínica Dental en el centro de Tarragona, siempre con la premisa de ejercer su profesión desde la nobleza, la sensibilidad y la excelencia profesional, entendiéndola como un reto y a la vez como algo muy humano. Los excelentes resultados en los más de 15.000 pacientes tratados por la Doctora avalan su trayectoria, siendo ésta una gran motivación para realizar su labor con entrega y orgullo cada día.